
- This event has passed.
โครงการอบรมเชิงปฏิบัติการเพื่อพัฒนาศักยภาพผู้ปฏิบัติงานเกี่ยวกับยาผลิตภัณฑ์การแพทย์ขั้นสูง Course No. 2.2 : ATMP Manufacturing (หลักสูตรด้านกระบวนการผลิต ATMP ขั้นสูง)
สิงหาคม 16, 2023 - สิงหาคม 17, 2023

โครงการอบรมเชิงปฏิบัติการเพื่อพัฒนาศักยภาพผู้ปฏิบัติงานเกี่ยวกับยาผลิตภัณฑ์การแพทย์ขั้นสูง
Course No. 2.2 : ATMP Manufacturing (หลักสูตรด้านกระบวนการผลิต ATMP ขั้นสูง)
 กำหนดการประชุมใหม่ 16 – 17 สิงหาคม 2566
กำหนดการประชุมใหม่ 16 – 17 สิงหาคม 2566
ณ ห้องจามจุรี 1 โรงแรมปทุมวัน ปริ๊นเซส กรุงเทพมหานคร
หลักกการและเหตุผล
ผลิตภัณฑ์การแพทย์ขั้นสูง (Advanced Therapy Medicinal Products; ATMPs) ซึ่งนิยมเรียกในประเทศในยุโรป หรือเซลล์และยีนบำบัด (Cellular and Gene Therapy, CGT) ซึ่งเป็นคำที่นิยมเรียกในสหรัฐอเมริกา ประกอบด้วยเซลล์ที่มีชีวิต ยีนหรือสารพันธุกรรม และเซลล์หรือเนื้อเยื่อสิ่งมีชีวิตที่สามารถใช้ฟื้นฟู ซ่อมแซม และทดแทนเนื้อเยื่อในร่างกายมนุษย์ ATMPs จัดเป็นยาที่มีชีวิต (living drugs) สามารถเพิ่มจำนวน ตอบสนองต่อตัวกระตุ้นต่างๆ และเปลี่ยนแปลงคุณสมบัติในร่างกายผู้ป่วยได้ การผลิต ATMPs/CGT ต้องทำภายใต้กระบวนการผลิตที่จำเพาะต่อบุคคล โดยการเก็บเซลล์จากผู้ป่วย ก่อนจะถูกส่งไปยังสถานที่ผลิตเพื่อผ่านกระบวนการผลิต และส่งกลับมายังโรงพยาบาลเพื่อบริหารยาแก่ผู้ป่วย ปัจจุบันมีการใช้ยากลุ่มนี้รักษาโรคมะเร็ง และแก้ไขความผิดปกติทางพันธุกรรมที่ไม่สามารถรักษาด้วยวิธีอื่นมาก่อน
ในประเทศไทย มีนักวิจัยจำนวนมากที่ทำงานที่เกี่ยวข้องกับการพัฒนาและวิจัยผลิตภัณฑ์ ATMPs/CGT ซึ่งรวมถึงผลิตภัณฑ์ที่เกี่ยวกับเซลล์บำบัด สเต็มเซลล์ หรือเซลล์ต้นกำเนิด ผลิตภัณฑ์เหล่านี้ถูกจัดเป็นยา ตามพระราชบัญญัติยา พ.ศ. 2510 แก้ไขเพิ่มเติมฉบับที่ 6 พ.ศ. 2562 เนื่องจากธรรมชาติของยาในกลุ่มนี้มีความแตกต่างจากยาเคมี และยาชีววัตถุทั่วไป จึงมีความจำเป็นที่จะต้องมีแนวทางที่ชัดเจนในการขึ้นทะเบียนผลิตภัณฑ์ ATMPs/CGT ซึ่งที่ผ่านมาสำนักงานคณะกรรมการอาหารและยา (อย.) ได้มีประกาศสำนักงานคณะกรรมการอาหารและยา เรื่อง การควบคุม กำกับ ดูแลยาที่เป็นผลิตภัณฑ์การแพทย์ชั้นสูง ประกาศ ณ วันที่ 7 มีนาคม 2561 และประกาศสำนักงานคณะกรรมการอาหารและยา เรื่อง แนวทางการขึ้นทะเบียนตำรับยาที่เป็นผลิตภัณฑ์การแพทย์ขั้นสูง ชนิดผลิตภัณฑ์เซลล์บำบัด ประกาศ ณ วันที่ 10 พฤษภาคม 2561
จากร่างการศึกษาวิจัยเชิงลึกในปี พ.ศ. 2564 พบว่ายังมีความต้องการส่งเสริมให้เกิดธุรกิจ บริการ และอุตสาหกรรม โดยเฉพาะระบบนิเวศในช่วง TRL 5-9 อย่างจริงจัง เพื่อเป็นการเตรียมความพร้อมรองรับการคิดค้นพัฒนาและยาในกลุ่มนี้สำหรับนักวิจัย และหน่วยงานที่มีหน้าที่กำกับดูแลผลิตภัณฑ์ ATMPs/CGT มีความจำเป็นอย่างยิ่งที่จะต้องมีการเตรียมความพร้อมบุคลากร นักวิจัย และผู้มีหน้าที่อนุมัติทะเบียนยา ให้มีความรู้เกี่ยวกับการเตรียมข้อมูลสำหรับขึ้นทะเบียนผลิตภัณฑ์กลุ่มนี้ ตลอดจนการพัฒนาแนวทางการขึ้นทะเบียนยากลุ่มนี้ให้มีความชัดเจน ปฏิบัติได้ โดยคำนึงถึงความเสี่ยงและประโยชน์ที่ประชาชนจะได้รับโดยไม่ประณีประนอมกับความไม่ปลอดภัยที่พึงจะเกิดขึ้น การเตรียมความพร้อมบุคลากรที่เกี่ยวข้องในวงจรชีวิตผลิตภัณฑ์ ATMPs/CGT ตลอดจนการพัฒนากฎเกณฑ์ และแนวทางการขึ้นทะเบียนยาเป็นการเตรียมความพร้อม ให้งานวิจัย และอุตสาหกรรมด้านนี้เติบโตได้อย่างรวดเร็ว และทันต่อสถานการณ์ เป็นการช่วยให้ประเทศไทยสามารถพึ่งพาตนเองได้ ประหยัดงบประมาณในการนำเข้าผลิตภัณฑ์ยา และยังส่งเสริมให้เกิดการส่งออกผลิตภัณฑ์ไปยังประเทศอื่นเพื่อนำรายได้เข้าประเทศอีกด้วย
เพื่อเป็นการเตรียมความพร้อมสำหรับงานคิดค้น พัฒนาและวิจัย และการกำกับดูแลผลิตภัณฑ์ ATMPs/CGT ของประเทศไทย โครงการนี้จึงมีวัตถุประสงค์ที่จะพัฒนาศักยภาพของนักวิจัย บุคลากรในอุตสาหกรรมยา และบุคลากรของหน่วยงานกำกับดูแลผลิตภัณฑ์สุขภาพในการปฏิบัติงานเกี่ยวกับการวิจัยและพัฒนา การขึ้นทะเบียนตำรับยารวมถึงการกำกับดูแลผลิตภัณฑ์การแพทย์ขั้นสูง เพื่อสนับสนุนให้เกิดการพัฒนาและผลิตผลิตภัณฑ์การแพทย์ขั้นสูงภายในประเทศและเพิ่มโอกาสในการแข่งขันกับต่างประเทศ
วัตถุประสงค์
1. เพื่อให้นักวิจัย บุคลากรในอุตสาหกรรมยา และบุคลากรของหน่วยงานกำกับดูแลผลิตภัณฑ์สุขภาพมีความรู้ความเข้าใจเกี่ยวกับการพัฒนาผลิตภัณฑ์การแพทย์ขั้นสูงตามแนวทาง ICH Q8
2. เพื่อให้นักวิจัย บุคลากรในอุตสาหกรรมยา และบุคลากรของหน่วยงานกำกับดูแลผลิตภัณฑ์สุขภาพมีความรู้ความเข้าใจเกี่ยวกับแนวทางการขึ้นทะเบียนตำรับยาที่เป็นผลิตภัณฑ์การแพทย์ขั้นสูงทั้งในและต่างประเทศ
3. เพื่อให้นักวิจัย บุคลากรในอุตสาหกรรมยา และบุคลากรของหน่วยงานกำกับดูแลผลิตภัณฑ์สุขภาพมีความรู้ความเข้าใจเกี่ยวกับระบบคุณภาพ รวมทั้งแนวปฏิบัติที่เกี่ยวข้องกับการผลิตรวมถึงการจัดเก็บและกระจายผลิตภัณฑ์การแพทย์ขั้นสูง
4. ส่งเสริมและสนับสนุนให้เกิดการจัดการความรู้ที่เกี่ยวกับการขึ้นทะเบียนตำรับยาที่เป็นผลิตภัณฑ์การแพทย์ขั้นสูงของประเทศไทย
อัตราค่าลงทะเบียน
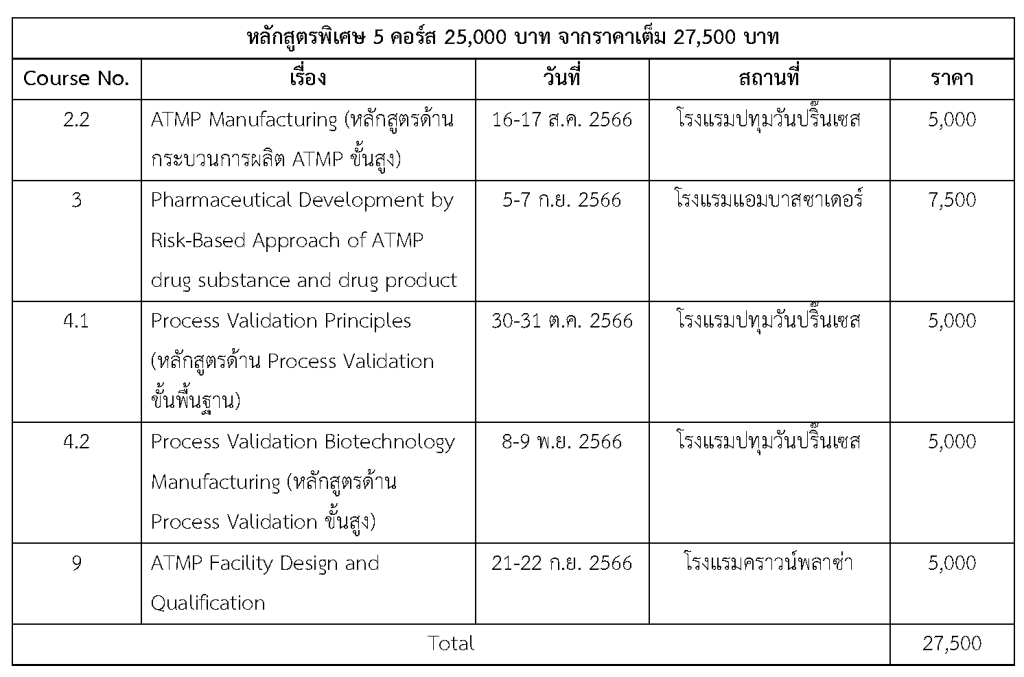
1. Course No.2.2 จำนวน 5,000 บาท
2. Coures พิเศษ จำนวน 25,000 บาท
วิธีการชำระเงิน

1. ลงทะเบียน https://bit.ly/3ITF75N_Registration
2. ส่งหลักฐานการชำระค่าลงทะเบียน https://bit.ly/ATMPManufacturing_Payments
3. ตรวจสอบรายชื่อการลงทะเบียนและสถานะ https://bit.ly/ATMP_Checklists